ALS、アルツハイマー病の早期診断に向けた新たな技術開発
~病因タンパク質TDP-43、アミロイドβを超高感度で検出可能に~
2024年10月9日
ALS、アルツハイマー病の早期診断に向けた新たな技術開発 ~病因タンパク質TDP-43、アミロイドβを超高感度で検出可能に~
【本研究のポイント】
・TDP-43 1)およびアミロイドβ 2)凝集体の超高感度検出法を開発
・界面活性剤Brij-58 3)の特異な性質を活用し、従来のSAA法 4)を大幅に改良
・従来の検出限界をはるかに上回る、最小5フェムトグラムからの検出を実現
・ALS、アルツハイマー病の早期診断や早期治療介入に貢献する可能性
岐阜大学大学院連合創薬医療情報研究科の本田諒准教授、大学院医学系研究科の下畑享良教授、岐阜薬科大学の位田雅俊教授らのグループは、神経変性疾患の発症に関わるTDP-43およびアミロイドβ凝集体の超高感度検出技術を開発しました。この技術は、新たに発見された「Brij-58」という特異な性質をもつ界面活性剤を使用することによって、従来のシード増幅アッセイ法(SAA法)の検出感度を飛躍的に向上させたものです。この技術により、最小5フェムトグラムという超微量の凝集体の検出が実現し、実際の患者の脳組織に蓄積した病的凝集体を検出することも可能となりました。本技術は、将来的にはALSなどの神経変性疾患の早期診断や早期治療介入に貢献することが期待されます。
本成果は、日本時間2024年10月8日にTranslational Neurodegeneration誌のオンライン版で発表されました。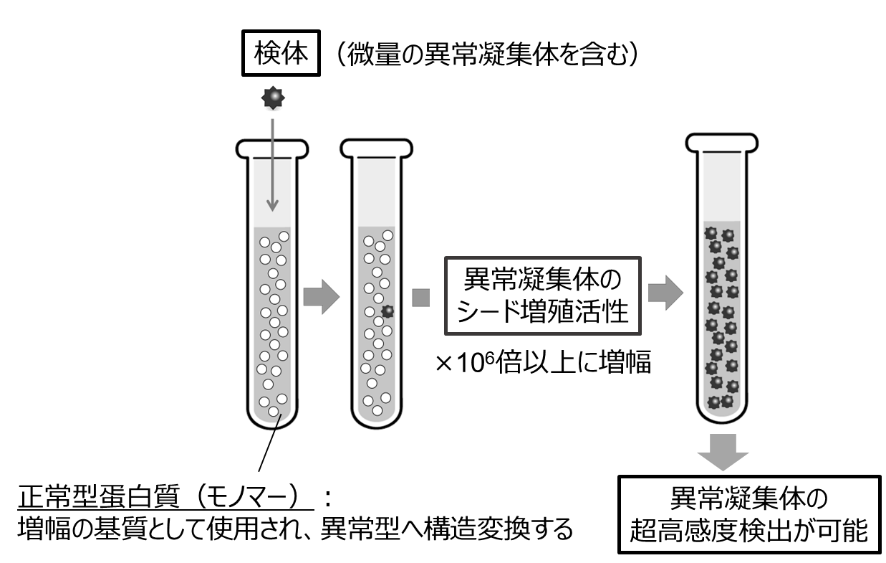
概略図: SAA法は患者の脳組織、脳脊髄液、血液などに含まれる超微量の病的凝集体を試験管内で「増やす」ことによって、これらを超高感度で検出する技術である。本研究では、従来技術を大幅に改良することで、TDP-43およびアミロイドβ凝集体の超高感度検出を実現した。
【研究背景】
神経変性疾患は、アルツハイマー病や筋萎縮性側索硬化症(ALS)、前頭側頭型認知症(FTLD)などのように、脳や神経系が徐々に損傷されていく病気です。これらの疾患に共通する特徴の一つが、異常なタンパク質の凝集体の蓄積です。TDP-43はALSとFTLD、アミロイドβはアルツハイマー病の原因物質として広く知られており、これらの異常凝集体が神経細胞の損傷を引き起こすことが示唆されています。このような背景から、病的な異常凝集体を高感度で検出する手法の開発が重要視されています。
シード増幅アッセイ(SAA)法は異常凝集体を試験管内で増幅することによって、これらを超高感度で検出する技術です。この技術はプリオン病やパーキンソン病で蓄積する異常凝集体を検出することが可能であり応用研究が進んでいますが、TDP-43やアミロイドβの異常凝集体に関しては十分な検出精度がありませんでした。これらの病的タンパク質の検出においては、反応基質となる正常型モノマーが非常に不安定ですぐに失活してしまうため、従来技術では異常凝集体の十分な増幅を起こすことができませんでした。従来法での検出限界はおよそ15ピコグラムであり、この精度では病理学的に有意な微量の凝集体を捉えるには不十分でした。そこで本研究では、新たなタンパク質の安定化技術を検索することによって、異常凝集体を効率よく試験管内で増幅し、検出する手法を検討しました。
【研究成果】
今回の研究の中心的成果の一つとして、新たな界面活性剤「Brij-58」の発見が挙げられます。Brij-58は、本研究で行った界面活性剤のスクリーニングから見出されました。この界面活性剤は、TDP-43やアミロイドβのモノマーを安定化させつつ、凝集体のシード増幅を阻害しないという特異な性質を持ちます。このため、病的凝集体の試験管内増幅と高感度検出に特に優れた効果を持ちます(図1)。

図1:Brij-58の作用メカニズムを示す図。(I)従来のSAA法では、反応基質となる正常型タンパク質(モノマー)が不安定な場合は、凝集体のシード増幅がうまく起こらないという欠点があった。(II)本研究では、Brij-58を正常型タンパク質(モノマー)に結合させ、安定なミセル構造を形成させることによって、この欠点を克服した。
Brij-58を従来のSAA法に組み入れることで、TDP-43の病的凝集体をわずか5フェムトグラムという微量から検出することに成功しました(図2)。これは従来の検出限界の数千倍に相当します。また、アミロイドβに対しても同様に高い検出感度が認められ、従来法の百倍以上の検出限界の向上が得られました。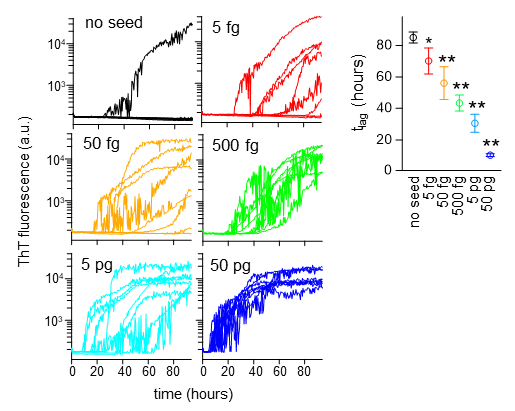
図2:本技術の検出精度を示す図。最小5フェムトグラムのTDP-43病的凝集体を試験管内で増幅し、検出することに成功した。
さらに、実際の患者から採取した脳組織を用いた検証実験でも、この新しい手法が高い精度で病的凝集体を検出できることが確認されました。図3に示すように、ALSとFTLDの患者の脳組織からTDP-43凝集体を検出し、健常者との明確な差異を確認することができました。この結果により、神経変性疾患の早期診断に向けた新たな検出技術として大きな可能性を示すことができました。
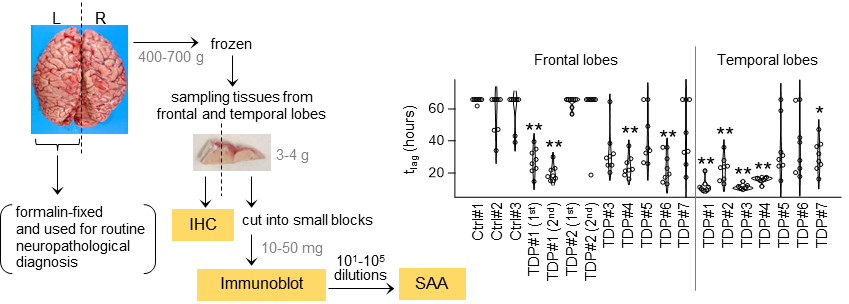
図3:患者から採取した脳組織を用いた検証実験の結果を示した図。病理組織学的にTDP-43の蓄積を確認した7例の脳組織(TDP#1-#7)からは病的凝集体が検出されたが、陰性対照となる正常患者の脳組織(Ctrl#1-#3)からは検出されなかった。
【今後の展開】
今回の研究成果は、神経変性疾患の早期診断や病態解明に向けた大きな一歩です。特に、本技術はTDP-43やアミロイドβの微量な凝集体を超高感度で検出できることから、疾患の発症前に異常なタンパク質の蓄積を検出し、早期治療介入に貢献できる可能性があります。現在、今回開発された技術を活用し、臨床現場で採取した血液や脳脊髄液からTDP-43の病的凝集体を検出する研究を進めています。
また、本研究で開発したBrij-58を基盤とするSAA法は、他の病的凝集体の検出にも応用できると考えられます。例えば、病的凝集体のひとつであるFUSも、TDP-43やアミロイドβと同様に、従来のSAA法では検出が難しい性質を有しています。本技術を広くさまざまな病的凝集体の検出に応用するために、さらなる感度向上に向けた技術改良も進めています。
本研究は、せりか基金-宇宙兄弟ALSプロジェクト-、公益信託宮田幸比古記念ALS研究助成基金、科研費(JP23K06935、JP22K07359、JP22K06744)の支援を受けて行われました。オープンアクセス化に関して、オープンアクセス加速化事業(文部科学省補助金)(東海国立大学機構 岐阜大学)の支援を受けました。
【用語解説】
1)TDP-43: 筋萎縮性側索硬化症、前頭側頭型認知症などに関連する異常なタンパク質の一種。
2)アミロイドβ: アルツハイマー病などに関連する異常なタンパク質の一種。
3)Brij-58: 界面活性剤の一種で、本研究でSAA法の検出感度を飛躍的に向上することが明らかになった。
4)SAA法:シード増幅アッセイ法、もしくはSeed Amplification Assay法。病的なタンパク質凝集体を試験管内で増幅することで、超高感度検出を可能とする技術である。プリオン病、パーキンソン病の早期診断法への応用研究が進んでいるが、TDP-43やアミロイドβ凝集体の検出は困難であった。
【論文情報】
雑誌名:Translational Neurodegeneration
論文タイトル:Ultrasensitive detection of TDP-43 and amyloid-β protein aggregates using micelle-assisted seed amplification assay
著者:Sora Sakamoto, Yuichi Riku, Teiko Komori Nomura, Akio Kimura, Naoki Yamahara, Kazuki Ohuchi, Mari Yoshida, Yasushi Iwasaki, Takayoshi Shimohata, Masatoshi Inden, and Ryo Honda
DOI: https://doi.org/10.1186/s40035-024-00444-7
【研究者プロフィール】
坂本空(筆頭著者)
岐阜薬科大学 医療薬剤学大講座 薬物治療学研究室 6年生
下畑享良
岐阜大学 大学院医学系研究科 脳神経内科学分野 教授
岐阜大学 高等研究院 One Medicine トランスレーショナルリサーチセンター (COMIT) (兼任)
位田雅俊
岐阜薬科大学 医療薬剤学大講座 薬物治療学研究室 教授
本田諒(責任著者)
岐阜大学 大学院連合創薬医療情報研究科 准教授
岐阜大学 高等研究院 One Medicine トランスレーショナルリサーチセンター (COMIT) (兼任)
岐阜薬科大学 医療薬剤学大講座 薬物治療学研究室 客員共同研究員(兼任)


.jpg)
-1.jpg)
_クレジット追加.jpg)
.jpg)




