新たな機序を活用した心房細動向け治療機器 「VARIPULSE® Platform」薬事承認を取得
パルスフィールドアブレーション技術(PFA)を採用したカテーテルアブレーション製品としては日本初の承認
2024年1月9日
ジョンソン・エンド・ジョンソン株式会社
メディカル カンパニー
新たな機序を活用した心房細動向け治療機器 「VARIPULSE® Platform」薬事承認を取得
パルスフィールドアブレーション技術(PFA)を採用した
カテーテルアブレーション製品としては日本初の承認
3次元マッピング技術を搭載し、合併症の低減をサポートする新たなテクノロジー
ジョンソン・エンド・ジョンソン株式会社 メディカル カンパニー(本社:東京都千代田区、代表取締役プレジデント:玉井 孝直、以下「ジョンソン・エンド・ジョンソン メドテック」)のバイオセンス ウェブスター事業部は、パルスフィールドアブレーション技術(PFA)を採用したアブレーションプラットフォーム「VARIPULSE® Platform(バリパルス® プラットフォーム)」が2023年12月22日に薬事承認されたことをお知らせいたします。PFAは熱的影響に依存せずにアブレーションすることが期待される、新しいテクノロジーです。PFAを採用した心房細動治療製品としては、日本で初めての承認となります。
「VARIPULSE® Platform」は、心房細動の根治を目指した治療、カテーテルアブレーション(経皮的カテーテル心筋焼灼術)に用いる製品群で、ソフトウェア、ジェネレータ、カテーテルで構成されています。カテーテルアブレーション治療は、不整脈の一種である心房細動の発生に関連する心房筋細胞を細胞死させ、心拍を正常なリズムに戻すことを目的に実施します。現在カテーテルアブレーションは、高周波通電や冷凍などの技術が採用されています。今回承認を受けた本製品は、短時間パルスで高電圧をかけることによりパルス電場を発生させ、細胞膜表面に生じさせた不可逆的な穿孔により細胞死を引き起こす熱的影響に依存しないPFAを用いているのが特徴です。心筋は細胞死を起こす閾値が低いため、ターゲットとする心筋細胞のみを選択的にアブレーションすることが期待できること、また、熱に依存しない技術により、食道や横隔膜などの心臓周辺臓器への損傷を抑え、合併症低減をサポートすることが期待されています。
また、本製品は不整脈治療の診断および治療のすべてのフェーズで手術をサポートする、当社の不整脈診断・治療機器システム「バイオセンスCARTO 3」※1専用製品として開発されており、従来通り、3次元マッピングシステムにより、立体構造である心房内を可視化しながら施術を行うことが可能です。
「VARIPULSE® Catheter」
(バリパルス® カテーテル)

「TRUPULSE® Generator」
(トゥルパルス® ジェネレータ)
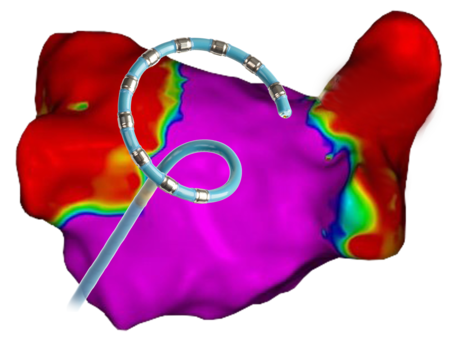
3次元マッピングシステム上での
「VARIPULSE® Platform」使用イメージ(合成)
心房細動の患者数は年々増加しており、国内では100万人※2を、世界では3750万人超えると推定されています※3。2030年までにさらに70%の増加が見込まれている※4中で、医療技術の向上に対する医療従事者の期待は高まっています。
■日本不整脈心電学会 理事長 清水渉 先生(日本医科大学大学院医学研究科循環器内科学分野 教授)コメント
心房細動におけるカテーテルアブレーション治療の技術革新は目覚ましく発展しています。この度、パルスフィールドアブレーション技術を採用したアブレーション治療が国内で承認されたことは、不整脈治療のさらなる進化を示すことになるでしょう。これまでもアブレーション治療を支えてきた3次元マッピングシステムに統合される新しいエネルギーソースによるカテーテルアブレーションは、さらに高度な治療を実現するとともに安全性のさらなる向上につながることが期待されています。
治療技術の多様性が広がることは、心房細動の根治を目指す医療者にとって、患者さんのために、それぞれの患者さんの状態に合わせた治療選択肢を提供できる可能性を広げます。
■ジョンソン・エンド・ジョンソン メドテック
カーディオバスキュラー スペシャルティ ソリューションズ バイスプレジデント 大多和裕志 コメント
この度、日本で初めて、PFAを採用した心房細動治療製品の薬事承認が得られたことは、大変意義深いものと考えています。さらなる研究が求められる部分があるものの、近年の研究でPFAは従来の高周波通電カテーテルよりも安全性が高いことが示唆されており※5※6、今後さらなる製品ラインナップの拡充や研究により、本技術が普及し、治療選択肢が拡大することを期待しています。また、心房細動は脳卒中の原因ともなる疾患であることから、脳卒中の予防の観点からも、今後日本の医療に貢献できることを願っています。なお、「VARIPULSE® Platform」の薬事承認は、ジョンソン・エンド・ジョンソンの世界各国市場のなかで、日本が初めてとなります。
バイオセンス ウェブスター事業部は、心房細動のカテーテルアブレーション診断および治療の技術革新をリードし続けてきました。2011年に日本で販売を開始した「バイオセンス CARTO 3」は、3次元マッピングシステムとナビゲーションにより、複雑な立体構造である心房内でカテーテルアブレーションの可視化を実現します。当システムと連動する、操作性の高い治療用カテーテルは、心房の無秩序な電気信号を止めるために心筋の一部を焼灼する高周波通電カテーテルです。カテーテル先端で連続して円形に焼灼する技術(フォーカル型)を用い、合併症低減や治療時間短縮にも貢献しながら精度の高いアウトカムを実現し、心房細動の根治を目指す患者さんの回復に寄与してきました。
この度薬事承認された「VARIPULSE® Platform」のカテーテル「VARIPULSE® Catheter」(バリパルス® カテーテル)は、円周状の管に電極を複数備えた形状により、ターゲットとなる心筋に対してスムーズにアプローチし、治療時間の短縮に貢献することが期待されます。
これまで技術革新を重ねてきた当社の高周波を原理とした製品ポートフォリオにさらにPFA製品が加わることで、今後医療従事者が症状に合わせて適切な技術の選択をすることが可能になり、心房細動の根治治療の選択肢の拡大につながります。
ジョンソン・エンド・ジョンソン メドテックは、メドテックのリーディング企業として、予防から診断・治療・回復まで、人々の健康と幸せ(ウェルビーイング)全体に寄与するイノベーションで、医療における包括的なソリューションを創出していきます。そして、スマート化・個別化・低侵襲化のソリューションを通じて、超高齢社会における医療やヘルスケアのあり方を再構想します。
--------------------
【心房細動とは】 心房細動とは、心房といわれる心臓上部の部屋が小きざみに震えて十分に機能しなくなる不整脈の一種で、脳梗塞などの合併症を起こすリスクがあります。健診結果データから、国内の心房細動の患者数は約100万人と推計されており、超高齢社会の日本では、心房細動の患者数は今後も増加し続けると予測されています。主な症状として、動悸、めまい、脱力感、胸の不快感、呼吸しにくい感じがすることがあげられます。一方で自覚症状がないケースもあり、その場合はさらに疾患の発見がしにくいため、心不全や心原性脳梗塞予防のためにも、心房細動の早期診断と治療が必要とされています。
--------------------
【心房細動の治療について】 心房細動の治療には大きく分けて薬物治療と非薬物治療の2つのアプローチがあります。薬による治療は、服用し続けることで不整脈の症状を抑えたり、正常の拍動に戻したりすることを目的としています。一方、非薬物治療のカテーテルアブレーション治療は、不整脈の根治を目指す治療法です。この療法は低侵襲的処置であり、カテーテルと呼ばれる細い管を、主に脚の付け根にある太い血管(大腿静脈ないし大腿動脈)から入れ、心臓まで到達させ、心筋のうち不整脈の原因となっている異常電気信号を受ける部分を細胞死させることによって、心房細動を引き起こす異常な電気信号の伝導を止める治療法です。
--------------------
【パルスフィールドアブレーションプラットフォーム 「VARIPULSE® Platform」 製品概要】
■アブレーション向け循環器用カテーテル 「VARIPULSE® Catheter」(バリパルス® カテーテル)
患者さんの心臓の形に合わせて先端のサイズ調整が可能であり、3次元マッピングシステムと統合可能な焼灼カテーテルです。
販売名:VARIPULSEパルスフィールドアブレーションカテーテル
承認番号:30500BZX00294000
■経皮心筋焼灼術用電気手術ユニット 「TRUPULSE® Generator」(トゥルパルス® ジェネレータ)
パルス電解フィールドを作るために超高速パルス電圧を発生させます。
販売名:TRUPULSEジェネレータ
承認番号:30500BZX00295000
【ジョンソン・エンド・ジョンソン株式会社 メディカル カンパニー(ジョンソン・エンド・ジョンソン メドテック)について】
ジョンソン・エンド・ジョンソン メドテックは、医療・ヘルスケア領域における多様な専門性、価値あるテクノロジー、人への情熱を最大限活かして、医療の将来を変革し、人々がその人にとって最もよい人生を送れるよう取り組んでいます。1世紀以上にわたり、私たちはサイエンスに基づく革新的なイノベーションの力で、アンメットニーズに応え、ヘルスケアを再構想してきました。私たちは、これからも、外科手術一般、整形外科、循環器科の領域において、人々の命を救うために、よりスマートで、低侵襲で、個別化されたヘルスケアソリューションの未来をリードしていきます。
【バイオセンス ウェブスター事業部について】
Biosense Webster Inc.は、不整脈の診断と治療を支える、科学およびテクノロジーのグローバルリーディングカンパニーです。専門性の高い医療テクノロジー企業である当社は、ジョンソン・エンド・ジョンソンの一員であり、カリフォルニア州アーバインに本社を置き、不整脈の診断や治療を支援する先進的な医療機器やソリューションを提供しています。詳細はwww.biosensewebster.com をご参照ください。(LinkedIn/Twitter)
ジョンソン・エンド・ジョンソン株式会社メディカル カンパニーのバイオセンス ウェブスター事業部は、心臓疾患のうち、頻脈性不整脈の診断に使用する 3D マッピングシステムや、カテーテルアブレーション(心筋焼灼術)という治療に使用する電極カテーテルなどを取り扱っています。
© Johnson & Johnson K.K. 2024. All rights reserved.
管理番号:JP_BWI_ALLB_301888
※1 「バイオセンスCARTO 3」(医療機器承認番号:22200BZX00741000)は、心臓内の 電気⽣理学的情報と3次元の解剖学的情報をシステム上でリアルタイムに統合した3Dマッピング画像を⽣成し、頻脈性不整脈の診断から治療までをサポートする医療機器です。磁界と電界を利⽤した「ACL Advanced Catheter Location テクノロジー」により、心臓内に挿⼊した電極カテーテルを画⾯上で視覚化することで、術者のカテーテル操作を⽀援します。システムに対応する治療⽤カテーテルを⽤いることで、頻脈性不整脈のカテーテルアブレーション治療を⽀援します。また、当社が提供する最新のモジュールのインストール、また周辺ツールの導⼊で、最新のマッピングテクノロジーを使⽤することができます。
※2 Inoue H, et al. Int J Cardiol 2009;137:102-107.
※3 Lippi G, Sanchis-Gomar F, Cervellin G. Global epidemiology of atrial fibrillation: An increasing epidemic and public health challenge. Int J Stroke. 2021;16(2):217-221. doi:10.1177/1747493019897870.
※4 Zoni-Berisso M, Lercari F, Carazza T, Domenicucci S. Epidemiology of atrial fibrillation : European perspective. Clin Epidemiol 2014; 6:213-220.
※5 Duytschaever M, de Potter T, Grimaldi M et al. Paroxysmal Atrial Fibrillation Ablation Using a Novel Vaiable-Loop Biphasic Pulsed Field Ablation Catheter Integrated With a 3-Dimensional Mapping System: 1-Year Outcomes of the Multicenter inspIRE Study. Circ Arrhythm Electrophysiol. 2023 Mar;16(3):e011780.
※6 Di Biase L, Diaz JC, Zhang XD et al. Pulsed field catheter ablation in atrial fibrillation. Trends in Cardiovasc Med. 2022 Aug;32(6):378-387.
Cautions Concerning Forward-Looking Statements
This press release contains “forward-looking statements” as defined in the Private Securities Litigation Reform Act of 1995 regarding Johnson & Johnson K.K. Medical Company, the VARIPULSE® Platform. The reader is cautioned not to rely on these forward-looking statements. These statements are based on current expectations of future events. If underlying assumptions prove inaccurate or known or unknown risks or uncertainties materialize, actual results could vary materially from the expectations and projections of Biosense Webster, Inc., Johnson K.K. Medical Company and/or Johnson & Johnson. Risks and uncertainties include, but are not limited to: challenges and uncertainties inherent in product research and development, including the uncertainty of clinical success and of obtaining regulatory approvals; uncertainty of commercial success; manufacturing difficulties and delays; competition, including technological advances, new products and patents attained by competitors; challenges to patents; product efficacy or safety concerns resulting in product recalls or regulatory action; changes in behavior and spending patterns of purchasers of health care products and services; changes to applicable laws and regulations, including global health care reforms; and trends toward health care cost containment. A further list and descriptions of these risks, uncertainties and other factors can be found in Johnson & Johnson’s Annual Report on Form 10-K for the fiscal year ended January 1, 2023, including in the sections captioned “Cautionary Note Regarding Forward-Looking Statements” and “Item 1A. Risk Factors,” and in Johnson & Johnson’s subsequent Quarterly Reports on Form 10-Q and other filings with the Securities and Exchange Commission. Copies of these filings are available online at www.sec.gov, www.jnj.com or on request from Johnson & Johnson. None of Biosense Webster, Inc., Johnson K.K. Medical Company nor Johnson & Johnson undertakes to update any forward-looking statement as a result of new information or future events or developments.


.jpg)
-1.jpg)
_クレジット追加.jpg)
.jpg)




