光合成微生物の力でサステナブルな細胞培養を実現
-老廃物のアップサイクルで培養肉技術の課題解消への途を拓く-
2024年10月3日
早稲田大学
神戸大学
光合成微生物の力でサステナブルな細胞培養を実現 -老廃物のアップサイクルで培養肉技術の課題解消への途を拓く-
詳細は早稲田大学HPをご覧ください。
発表のポイント
● 乳酸を吸収する光合成微生物シアノバクテリアを動物細胞と共培養※1することで、相互に栄養素と老廃物を交換する培養システムを構築し、動物細胞の長期培養を実現
● 成長因子※2を分泌する動物細胞とシアノバクテリアを共培養した時に得られる培養上清液※3は、動物細胞を単独で培養した時に得られる上清液よりも3倍以上骨格筋芽細胞の増殖を促進
● 本培養上清液を用いることで培養肉※4生産の課題となっている動物血清の使用を削減できることを確 認。今後、培養肉生産だけでなく、精密発酵やバイオ医薬生産に応用することで、食料・医薬品の生産コストの削減および環境負荷低減に貢献の可能性
早稲田大学理工学術院の朝日透(あさひとおる)教授、同大大学院先進理工学研究科(一貫制博士課程)の秋尚雅(チュサンア)、および東京女子医科大学先端生命医科学研究所の清水達也(しみずたつや)教授、原口裕次(はらぐちゆうじ)特任准教授の研究グループは、神戸大学先端バイオ工学研究センターの蓮沼誠久(はすぬまともひさ)教授の研究グループと共同で、自浄作用および栄養循環を果たす食料生産システムを構築するため、光合成微生物を利用した新しい細胞培養システムを開発しました。
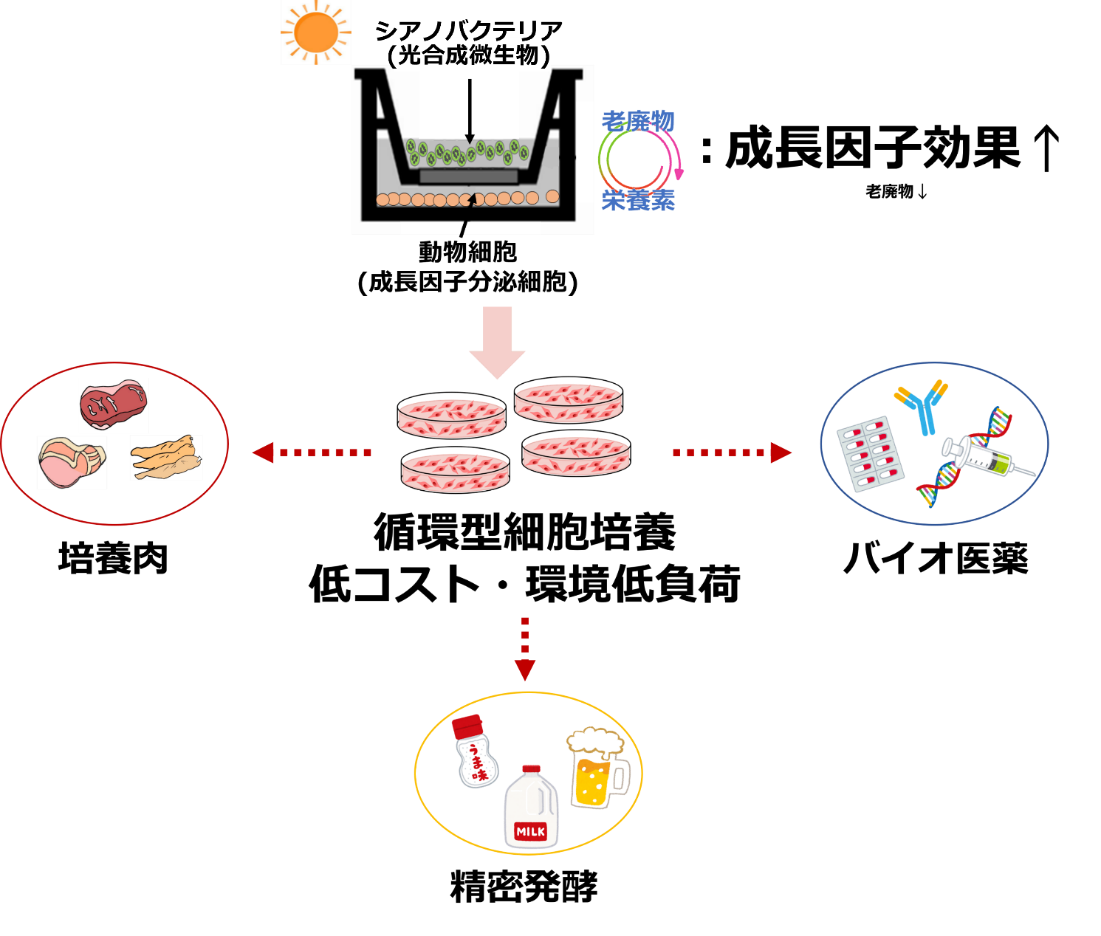
近年、持続可能な食肉生産技術として培養肉が注目されていますが、動物血清の使用や老廃物の蓄積および栄養枯渇により、多量の培養液使用とその廃液の発生が課題となっています。本研究では、動物細胞の代謝老廃物(乳酸・アンモニア)を栄養源(ピルビン酸・アミノ酸)に変換する光合成微生物のシアノバクテリアを成長因子分泌動物細胞と共培養することにより、動物血清を使用せず、さらに培養液の使用量を削減する低コストで低環境負荷の培養肉生産につながる細胞培養システムを実現しました。
本研究成果は、2024 年8月23日にネイチャー・パブリッシング・グループのオンライン総合科学誌『Scientific Reports』に発表されました。論文名:A serum-free culture medium production system by co-culture combining growth factor-secreting cells and L-lactate-assimilating cyanobacteria for sustainable cultured meat production
キーワード
培養肉、光合成、共培養、シアノバクテリア、成長因子、細胞増殖、培養システム、乳酸
(1)これまでの研究で分かっていたこと
培養肉は、2012年にオランダ・マーストリヒト大学のMark Post教授によって初めて提唱され、大豆ミートや昆虫タンパクと並ぶ代替タンパク質の一種として、世界中で研究・開発が進められています。現在では、174社以上の培養肉ベンチャーが立ち上がり、特にアメリカやシンガポールでは市場化が進んでいます。これに伴い、世界中の投資家や企業からの関心が高まり、培養肉分野には31億ドル規模の投資が行われ、今後さらなる拡大が期待されています。(参考文献1)
従来の培養肉生産において、動物筋肉細胞の増殖のために動物血清が不可欠でしたが、そのコストや動物倫理に対する懸念が問題視されていました。そのため、血清を使わず、動物筋肉細胞を増殖できる培養方法が求められています。血清には細胞の成長因子といったタンパク質が含まれ、これらは特定の動物細胞から分泌されていることがわかっています。先行研究(参考文献2)において、ラット肝臓細胞が分泌する成長因子を含む培養上清液が、血清を使わずに牛骨格筋芽細胞の増殖を促進することを発見しました。成長因子分泌細胞を長期間培養すれば多量の成長因子が得られる一方で、乳酸やアンモニアなどの老廃物が蓄積することで培養液の性能が低下する問題があります。そのため、成長因子分泌細胞の培養上清液の血清代替としての性能を高めるためには、老廃物の除去が不可欠となります。さらに長期間の培養は栄養素の枯渇をもたらします。先行研究(参考文献3)では、乳酸を取り込みピルビン酸に変換するリコンビナント※5シアノバクテリアを開発しました。
そこで、本研究グループでは、成長因子を分泌する細胞と乳酸などの老廃物を取り込み、かつ老廃物を栄養素に変換するシアノバクテリアを共培養する新たな培養システムを考案しました。それにより、動物血清を用いることなく効率的な筋肉細胞の増殖が実現するのではないかと考えました。
(2)今回新たに実現しようとしたこと、明らかになったこと、そのために新しく開発した手法
シアノバクテリアの一種であるシネココッカスは、光合成能力が高く、遺伝子組換え操作も容易で、さらに動物細胞に対して優れた生体適合性を持つことから、さまざまな分野で利用されています。本研究で使用したL-乳酸を取り込むシアノバクテリアも、シネココッカスのリコンビナント株であり、動物細胞の老廃物である乳酸とアンモニアを動物細胞の栄養素となるピルビン酸とアミノ酸に変換する能力は、先行研究(参考文献2)で確認されていました。しかし、動物細胞と共培養を行った時にも、この機能が発揮されるかは未知のままでした。
本研究で、このシアノバクテリアと成長因子を分泌するラット肝臓細胞を共培養すると、培養条件を最適化することで、シアノバクテリアが乳酸を3割以上、アンモニアを9割以上減少させることを確認しました。さらに、シアノバクテリアによって産生されたピルビン酸やアミノ酸は、動物細胞によって利用される量よりも多く、結果として培養上清液中に栄養源が多く残存していることが明らかになりました。この上清液を用い、血清を使わずに骨格筋芽細胞を増殖させたところ、その増殖率はラット肝臓細胞の単独培養上清液と比較して3倍以上であることを確認しました。すなわち、シアノバクテリアとの共培養を行うことで、成長因子分泌細胞の培養上清液の血清代替としての性能を高めることに成功しました。
(3)研究の波及効果や社会的影響
この研究は、動物血清を使用せず、また培養液の使用量を低減可能な動物細胞培養法につながることから、培養肉生産のコスト削減と環境負荷の低減に寄与する可能性があります。動物細胞と光合成微生物を原料とし、動物を使用しない食肉生産技術として、将来的に食料問題や動物倫理、気候変動の課題解決に貢献することが期待されます。また、この細胞培養システムは、培養肉だけでなく、バイオ医薬品生産や再生医療など、さまざまな細胞培養分野にも適用可能な汎用性を持っています。
(4)今後の課題
今後の課題としては、大量生産に向けて現在の平面培養システムを3次元培養システムにスケールアップし、それに応じた最適な培養条件を探索することが挙げられます。また、培養液の成分を網羅的に解析し、光合成微生物と動物細胞間の相互作用を解明することで、分子生物学的な知見を広げる研究にもつながります。
(5)研究者のコメント
本研究の最終目標は、このシステムを活用した安全で安価な培養肉の生産です。今回得られた研究成果を基盤に、動物だけでなく魚類などさまざまな筋肉細胞から効率的に培養肉を作り出す技術の確立を目指しています。今後も、3次元培養システムの開発や最適な培養条件の探求を通じて、実用化に向けたステップを踏んでいく予定です。
(6)用語解説・参考文献
※1 共培養
2種類以上の細胞を同じ培養液で一緒に培養することを指します。これにより、細胞間の相互作用が起こり、情報伝達物質や生理活性物質の分泌が向上する効果が期待されます。
※2 成長因子
細胞の増殖や分化を促進するタンパク質やペプチドのことです。成長因子は、細胞の情報伝達を刺激し、さまざまな生理的プロセスを制御します。
※3 培養上清液
細胞を培養した後の培養液を指します。この上清液には、細胞が分泌した成長因子やその他の分子(老廃物なども)が含まれ、細胞培養において正負両面(細胞の生存と増殖、細胞死・増殖停止の両側)にわたり重要な役割を果たします。
※4 培養肉
動物から採取した細胞を培養して、組織工学の技術を用いて作られる人工肉のことです。動物を直接屠殺することなく生産されるため、環境負荷や動物倫理に配慮した技術として注目されています。
※5 リコンビナント
遺伝子組換え技術を利用して作られた生物や物質を指します。特定の目的に応じて遺伝子操作を行い、新たな形質を持たせた微生物やタンパク質が「リコンビナント」として利用されます。
参考文献:
1.Good Food Institute. (2024). 2023 State of the Industry Report: Cultivated meat and seafood. Good Food Institute. Retrieved Sep. 26, 2024, from: https://gfi.org/wp-content/uploads/2024/04/2023-State-of-the-Industry-Report-Cultivated-meat-and-seafood.pdf
2. Yamanaka, K., Haraguchi, Y., Takahashi, H., Kawashima, I., & Shimizu, T. (2023). Development of serum-free and grain-derived-nutrient-free medium using microalga-derived nutrients and mammalian cell-secreted growth factors for sustainable cultured meat production. Scientific Reports, 13(1), 498.
3.Haraguchi, Y., Kato, Y., Inabe, K., Kondo, A., Hasunuma, T., & Shimizu, T. (2023). Circular cell culture for sustainable food production using recombinant lactate-assimilating cyanobacteria that supplies pyruvate and amino acids. Archives of Microbiology, 205(7), 266.
(7)論文情報
雑誌名:Scientific reports
論文名:A serum-free culture medium production system by co-culture combining growth factor-secreting cells and L-lactate-assimilating cyanobacteria for sustainable cultured meat production
執筆者名:秋尚雅(早稲田大学)、原口裕次 (東京女子医科大学)、朝日透(早稲田大学)、加藤裕一(神戸大学)、近藤昭彦(神戸大学)、蓮沼誠久(神戸大学)、清水達也*(東京女子医科大学)
掲載日時(日本時間):2024年8月23日
掲載URL:https://www.nature.com/articles/s41598-024-70377-8
DOI: 10.1038/s41598-024-70377-8
(8)研究助成
研究費名:内閣府ムーンショット型農林水産研究開発事業(管理法人:生物系特定産業技術研究支援センター)
研究課題名: 藻類と動物細胞を用いたサーキュラーセルカルチャーによるバイオエコノミカルな培養食料生産システム
研究代表者名(所属機関名):清水達也(東京女子医科大学)


.jpg)
-1.jpg)
_クレジット追加.jpg)
.jpg)




